
Строение атома. Кислород: Архитектура окисления. Часть 6
«Истину следует искать в простоте, а не в многообразии и путанице вещей»
— Исаак Ньютон
Мы продолжаем наше расследование. В прошлых частях мы увидели, как линейный Углерод создаёт жизнь, а асимметричный Азот создаёт напряжение.
Теперь мы переходим к Кислороду-16.
И здесь мы не будем просто описывать структуру. Мы сделаем то, что должна делать настоящая наука: мы предскажем химические свойства элемента, просто глядя на чертёж его ядра.
📐 Инженерный анализ ядра
Кислород-16 состоит из 8 протонов и 8 нейтронов. Это ровно 4 альфа-частицы. Вспомним нашу модель:
- Углерод — это цепочка из 3-х альфа-частиц.
- Кислород — это Углерод + 1 альфа-частица.
Куда встанет четвёртый блок? Природа всегда ищет компактность. Четвёртая альфа-частица крепится сверху к центру углеродной цепочки, образуя Т-образную структуру.
Создадим модель ядра Кислорода:
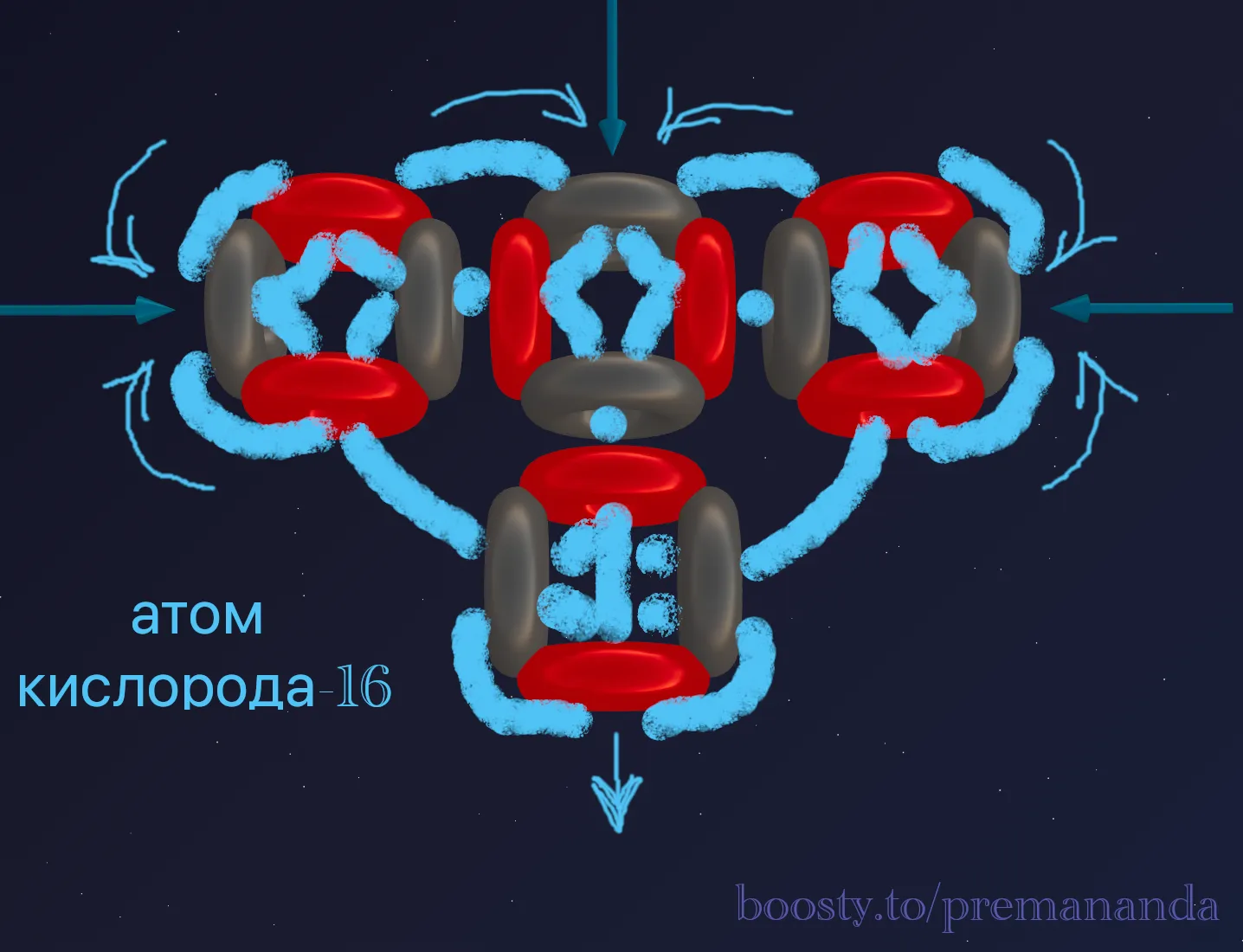
Что мы видим на чертеже?
- Вверху — две мощные воронки, направленные в стороны, и одна вверх.
- Снизу — один мощный фонтан.
🔮 Прогноз №1: Валентность 2 или 3
Глядя на Т-образную форму, мы можем сразу сказать, сколько связей образует этот атом. Самыми активными являются две воронки, направленные в стороны. Верхняя воронка тоже иногда может участвовать в реакциях.
Вывод: Кислород должен чаще соединяться двумя и, в некоторых случаях, тремя связями.
Реальность: Две связи в молекулах воды (H₂O) и фториде кислорода (OF₂). Три связи в H₃O⁺ (ион гидроксония). Наша модель предсказала это точно.
🔮 Прогноз №2: Электроотрицательность (Сила всасывания)
В химии есть понятие «электроотрицательность» — способность атома оттягивать на себя электроны. Кислород в этом чемпион (уступает только фтору). Почему?
Официальная наука вводит коэффициенты. Эфиродинамика объясняет механику. Посмотрите на ядро Кислорода. Это 4 мощных насоса (альфа-частицы). В отличие от цепочки Углерода, здесь присутствует асимметрия, которая обнажает входящие потоки.
Вывод: Этот атом будет работать как мощный пылесос, агрессивно срывая эфирные потоки (электроны) с соседей.
Реальность: Кислород — сильнейший окислитель, поддерживающий горение.
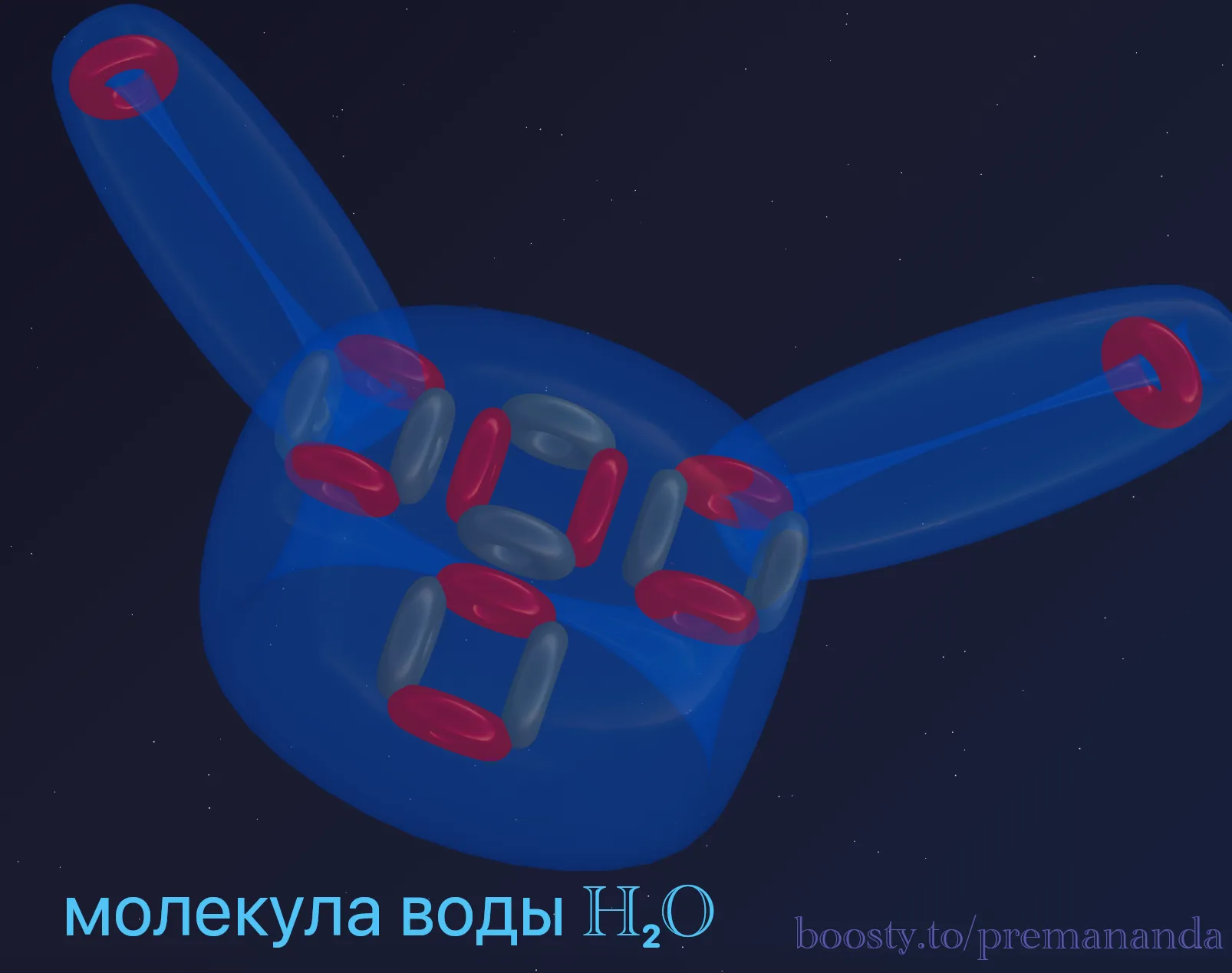
💧 Прогноз №3: Геометрия Воды (H₂O)
У нас есть два активных порта по бокам. К ним присоединяются два атома Водорода. Вспоминаем принцип гибких связей: водороды привязаны к воронкам, но отталкиваются друг от друга.
Однако, в отличие от Углерода, у Кислорода есть массивная «Корона» сверху. Этот вихрь давит на атомы водорода, не давая им выпрямиться в линию (на 180 градусов). Он прижимает их вниз. Баланс между «давлением короны» и «отталкиванием водородов» создаёт тот самый угол в 104,5 градуса.
🔗 Прогноз №4: Молекула O₂ (Двойная связь)
Что будет, если встретятся два атома Кислорода? У каждого из них по 2 активных порта. Они встают напротив друг друга и соединяются:
- Левый вихрь первого атома сцепляется с правым вихрем второго.
- Правый вихрь первого — с левым вихрем второго.
Образуется двойная связь.

Именно поэтому кислород (O₂) химически активен: двойную связь разорвать легче, чем тройную связь азота, и наш «пылесос» всегда готов переключиться на что-то более вкусное (окислить кого-нибудь).
🌟 Предсказательная сила эфиродинамики
Структура ядра — это чертёж, по которому строится химия. Т-образная форма ядра Кислорода (4 альфа-частицы) объясняет:
- Почему он двухвалентен (2 открытых воронки).
- Почему он мощный окислитель.
- Почему вода имеет угол 104,5° (воздействие 4-й альфа-частицы на присоединённые ядра).
- Почему он образует двойные связи (2 активных воронки).
Вывод: Мы не просто подгоняем факты под теорию — мы видим логику природы и можем предсказывать свойства элементов, глядя на архитектуру их ядер!
🔮 Что дальше?
В следующей части — Фтор:
- Самое агрессивное вещество во Вселенной.
- Как асимметрия превращает элемент в химического хищника.